Via libera all'immunoterapia Car-T tisagenlecleucel che utilizza i linfociti T per combattere le neoplasie. Potrà essere usata per il trattamento di due forme di leucemia e linfoma, nel caso non funzionino le terapie tradizionali.
Roma, 27 agosto 2018 - Novità importante nel campo della cura di leucemie e linfomi. La Commissione europea ha dato l'ok all'uso dell'immunoterapia Car-T tisagenlecleucel per il trattamento di bambini e giovani adulti fino ai 25 anni con leucemia linfoblastica acuta (Lla) a cellule B e per il trattamento di pazienti adulti con linfoma diffuso a grandi cellule B (Dlbcl) nei casi in cui la patologia non risponda alle tradizionali terapie (neoplasie recidivanti o refrattarie). E' la prima volta che la cura per i tumori chiamata 'Car T', che prevede l'uso delle cellule del paziente 'addestrate' a riconoscere quelle tumorali, arriva in Europa. Ad annunciarlo è la svizzera Novartis, che "continua a collaborare con le autorità competenti di tutta Europa - si legge in una nota - per definire un approccio economico equo e basato sul valore, ma che sia al contempo sostenibile per i servizi sanitari nazionali".
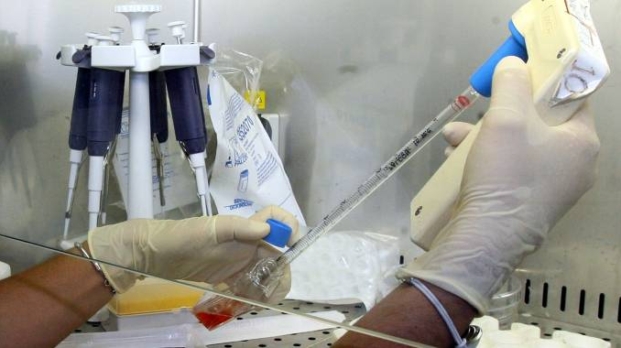
IN COSA CONSISTE LA CAR-T THERAPY- E' la stessa azienda a spiegare le potenzialià del nuovo farmaco sviluppato in collaborazione con l'università della Pennsylvania: "Tisagenlecleucel è un trattamento rivoluzionario cheutilizza i linfociti T del paziente per combattere il cancro". La Cart-t therapy consiste infatti nel prelevare i linfociti T del paziente, un tipo di cellule del sistema immunitario, modificandoli perché riconoscano le cellule tumorali e poi reinfondendoli dopo averli fatti replicare. E' anche "l'unica terapia con recettore antigenico chimerico delle cellule T (Car-T) che ha ricevuto l'approvazione regolatoria nella Ue per due distinte neoplasie a cellule B", nonché "è stato anche la prima terapia cellulare Car-T mai approvata dalla Fda statunitense".
IL SI' DELL'EMA - L'autorizzazione della Commissione è arrivata dopo il parere positivo del Chmp, il comitato dell'Ema (Agenzia europea per i medicinali) che si occupa dell'approvazione dei farmaci, a fine giugno. Per Liz Barrett, Ceo di Novartis Oncology, il via libera dell'Emarappresenta "una svolta trasformativa per i pazienti in Europa che hanno bisogno di nuove opzioni terapeutiche. Perseguendo tenacemente il suo obiettivo di ridisegnare la cura del cancro - aggiunge - Novartis sta realizzando un'infrastruttura globale per la fornitura di terapie cellulari Car-T, laddove prima non ne esisteva alcuna".
Peter Bader, capo della Divisione immunologia e trapianti di cellule staminali dell'University Hospital for Children and Adolescents di Francoforte, principal investigator dello studio 'Eliana' sul tisagenlecleucel, parla di "progresso senza precedenti del paradigma terapeutico". Il farmaco, evidenzia in particolare l'esperto, "costituisce una terapia salvavita per i giovani pazienti con Lla che non sono stati trattati con successo con le terapie esistenti e per i quali sono rimaste poche opzioni terapeutiche".
Nessun commento:
Posta un commento